塩化水銀(I)
| 塩化水銀(I) | |
|---|---|
 | |
IUPAC名 塩化水銀(I) | |
別称 甘汞、カロメル | |
| 識別情報 | |
CAS登録番号 |
10112-91-1 |
EC番号 |
233-307-5 |
国連/北米番号 |
|
RTECS番号 |
OV8750000 |
| 特性 | |
化学式 |
Hg2Cl2 |
モル質量 |
472.09 g/mol |
| 外観 |
白色の固体 |
密度 |
7.150 g/cm3 |
沸点 |
383 °C, 656 K, 721 °F (昇華) |
水への溶解度 |
0.2 mg/100 mL |
| 危険性 | |
安全データシート(外部リンク) |
ICSC 0984 |
EU分類 |
有害(Xn) 環境への危険性(N) |
| EU Index |
080-003-00-1 |
Rフレーズ |
R22, R36/37/38, R50/53 |
Sフレーズ |
(S2), S13, S24/25, S46, S60, S61 |
| 関連する物質 | |
| その他の陰イオン |
フッ化水銀(I) 臭化水銀(I) ヨウ化水銀(I) |
| その他の陽イオン |
塩化水銀(II) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
塩化水銀(I)(えんかすいぎん いち、calomel)は、水銀の塩化物の1つ。水銀の塩化物である塩化水銀は2種類あり、もう1つは塩化水銀(II) である。Hg2Cl2 という組成をもち、塩化第一水銀(えんかだいいちすいぎん)、甘汞(かんこう)、カロメルとも言う。水銀原子同士が共有結合により結合しているため HgCl とは表記しない。
目次
1 性質
2 構造
3 用途
4 脚注
5 外部リンク
性質
光に当たると塩化水銀(II) と金属水銀に分解する。毒性は塩化水銀(II)よりは弱いが、毒物および劇物取締法で劇物に指定されている。白色またはやや黄ばんだ白色をしていて水には溶けにくい。
アンモニア水と反応すると黒色に変わる。反応式は次の通りである。
- Hg2Cl2+2NH3⟶Hg+Hg(NH2)Cl+NH4++Cl−{displaystyle {ce {{Hg2Cl2}+2NH3->{Hg}+{Hg(NH2)Cl}+{NH4^{+}}+Cl^{-}}}}
構造
水銀は第12族元素では唯一 M-M 結合を形成する元素で、Cl-Hg-Hg-Clの単位構造をとる。
 |
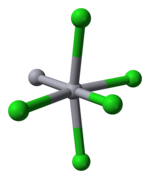 |
| 単位格子 | 八面体構造の球棒モデル |
Hg-Hgの結合長は253 pmで、Hg-Clの結合長は243 pmである[1]。全体的に水銀原子を中心とした八面体形構造をとり、2番目に近い4個の塩素原子との距離は321 pmである。
用途
かつては化粧品(白粉)や下剤・利尿剤として利用されていたが、水銀中毒の危険があるために現在は使用されていない。塩化水銀(I) は電極として利用されることがある。
脚注
^ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
外部リンク
- 塩化第一水銀
| ||||||||



