三フッ化ヒ素
| 三フッ化ヒ素 Arsenic trifluoride | |
|---|---|
 |  |
IUPAC名 Arsenic(III) fluoride | |
別称 フッ化ヒ素(III) | |
| 識別情報 | |
CAS登録番号 | 7784-35-2 |
PubChem | 24571 |
RTECS番号 | CG5775000 |
| 特性 | |
化学式 | AsF3 |
モル質量 | 131.9168 g/mol |
| 外観 | 無色の液体 |
密度 | 2.666 g/cm3[1] |
融点 | -8.5 ℃ |
沸点 | 60.4 ℃ |
水への溶解度 | 分解 |
アルコール、エーテル、ベンゼン、アンモニアへの溶解度 | 可溶 |
| 危険性 | |
主な危険性 | 毒性、腐食性 |
Rフレーズ | R23/25, R50/53 |
Sフレーズ | (S1/2), S20/21, S28, S45, S60, S61 |
| 熱化学 | |
標準生成熱 ΔfH | -305.0 kJ/mol |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
三フッ化ヒ素(さんフッかヒそ、英: arsenic trifluoride)はヒ素のフッ化物で、化学式AsF3で表される無機化合物。無色の液体で、水と容易に反応する[2]。半導体の製造などに使われる。
生成、性質
フッ化水素と三酸化二ヒ素の反応により生成される[2]。
- 6HF +As2O3⟶2AsF3 +3H2O{displaystyle {ce {6HF + As2O3 ->2AsF3 + 3H2O}}}
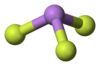
分子構造は三角錐形で、気体の状態では、ヒ素とフッ素の間の結合距離は170.6pm、結合角は96.2°となっている[3]。
非金属塩化物のフッ素化に使われるが、三フッ化アンチモンに比較すると反応性は劣る[2]。
四フッ化ヒ素セシウム(Cs2AsF4{displaystyle {ce {Cs2AsF4}}}

フッ化カリウムとの反応により、七フッ化二ヒ素カリウムを生成する。これは AsF3{displaystyle {ce {AsF3}}}

- KF +2AsF3⟶KAs2F7{displaystyle {ce {KF + 2AsF3 -> KAs2F7}}}
AsF2+{displaystyle {ce {AsF2^+}}}


安全性
日本の毒物及び劇物取締法では毒物に該当し、発癌性がある[7]。
脚注
^ Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 0070494398
- ^ abcGreenwood, Norman N.; Earnshaw, Alan. (1997), Chemistry of the Elements (2 ed.), Oxford: Butterworth-Heinemann, ISBN 0080379419
^ Wells A.F. (1984) Structural Inorganic Chemistry 5th edition Oxford Science Publications ISBN 0-19-855370-6
^ New alkali metal and tetramethylammonium tetrafluoroarsenates(III), their vibrational spectra and crystal structure of cesium tetrafluoroarsenate(III)Klampfer P, Benkič P, Lesar A, Volavšek B, Ponikvar M , Jesih A., Collect. Czech. Chem. Commun. 2004, 69, 339-350 doi:10.1135/cccc20040339
^ Alkali-metal heptafluorodiarsenates(III): their preparation and the crystal structure of the potassium salt, Edwards A.J., Patel S.N., J. Chem. Soc., Dalton Trans., 1980, 1630-1632, doi:10.1039/DT9800001630
^ Fluoride crystal structures. Part XV. Arsenic trifluoride–antimony pentafluoride, Edwards A. J., Sills R. J. C. J. Chem. Soc. A, 1971, 942 - 945, doi:10.1039/J19710000942
^ 安全衛生情報センター
| ||||


